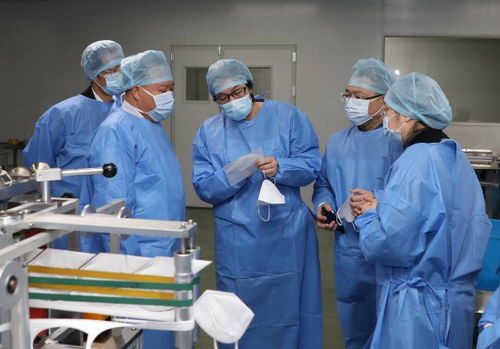
随着疫情的突发,许多企业积极响应号召转产医疗器械,尤其是第二类医疗器械(如医用口罩、防护服等),以满足公共卫生需求。转产过程中如何通过应急审批流程并确保产品质量安全,成为关键问题。以下从应急审批流程和安全保障两方面展开说明。
一、应急审批流程的优化与实施
为应对疫情,国家药品监督管理局已出台应急审批政策,简化第二类医疗器械的注册和备案程序。企业转产需遵循以下步骤:
1. 提交申请:企业需准备产品技术文件、生产资质证明和疫情相关需求说明,通过线上平台提交至省级药品监督管理部门。
2. 快速审核:监管部门优先处理,缩短审核时间,通常可在数周内完成,必要时可实行附条件审批,允许产品在严格监控下先行上市。
3. 现场核查:转产企业可能面临简化版现场检查,重点评估生产环境、设备能力和质量管理体系,确保基本合规。
4. 持续监督:获批后,企业需定期提交质量报告,并接受动态监管,以应对潜在风险。
应急审批流程旨在平衡效率与安全,企业应主动与监管部门沟通,避免因准备不足导致延误。
二、安全保障措施:从生产到销售的全链条管理
转产医疗器械不仅需快速获批,更需筑牢安全防线,确保产品有效可靠。以下是关键保障措施:
- 严格质量控制:企业应建立符合《医疗器械生产质量管理规范》的体系,包括原料采购、生产过程监控和成品检验。例如,转产医用口罩时,需确保过滤效率、生物相容性等指标达标,并定期自检或委托第三方检测。
- 人员培训与资质:转产往往涉及跨行业生产,企业需对员工进行医疗器械相关培训,特别是无菌操作和风险防控知识,必要时引进专业人才。
- 销售环节规范:第二类医疗器械销售需取得相应经营许可证,并建立追溯系统。企业应记录产品流向,确保可追踪到终端用户,同时加强售后服务,及时处理不良反应或投诉。
- 应急响应机制:企业需制定应急预案,如发现产品缺陷,立即启动召回程序,并与监管部门协作,最大限度降低公共健康风险。
企业在转产第二类医疗器械时,应充分利用应急审批流程的便利性,同时将安全置于首位。通过完善的质量管理和全链条监管,不仅能快速响应疫情需求,还能赢得市场信任,为公共卫生事业贡献力量。监管部门、企业和社会各方需协同努力,共同构建安全高效的医疗器械供应体系。